
Wir stehen für den Transfer von Wissenschaft in die Praxis
Die ChondroFiller® Produkte wurden in enger Zusammenarbeit unseres Teams mit Wissenschaftlern, Ärzten und mit Forschern des Fraunhofer-Instituts für Grenzflächen- und Bioverfahrenstechnik IGB in Stuttgart entwickelt. meidrix biomedicals hat daraus Produkte für die orthopädische Praxis gemacht. Und an dieser Stelle schließt sich die Klammer, denn selbstverständlich wurde und wird der Einsatz des ChondroFiller® sowohl in wissenschaftlichen als auch in klinischen Studien unabhängig untersucht.
Forschung und Entwicklung
Unsere jahrzehntelange Erfahrung mit Biomaterialien und regenerativer Medizin teilen wir gerne mit Kooperationspartnern aus dem klinischen, universitären und industriellen Bereich für innovative Forschungs- und Entwicklungsprojekte in einem weitreichenden Netzwerk.
Eine Übersicht über wissenschaftliche Studien erhalten Sie nachfolgend:
2016 | Stretching human mesenchymal stromal cells on stiffness-customized collagen type I generates a smooth muscle marker profile without growth factor addition.
Rothdiener, M., Hegemann, M., Uynuk-Ool, T., Walters, B., Papugy, P., Nguyen, P., Claus, V., Seeger, T., Stoeckle, U., Boehme, K. A., Aicher, W. K., Stegemann, J. P., Hart, M. L., Kurz, B., Klein, G., & Rolauffs, B. (2016). Stretching human mesenchymal stromal cells on stiffness-customized collagen type I generates a smooth muscle marker profile without growth factor addition. Scientific reports, 6, 35840.
2017 | Mechanobiological processes of tissue engineered cartilage replacement materials.
Nachtsheim, J., Markert, B. and Stoffel, M. (2017), Mechanobiological processes of tissue engineered cartilage replacement materials. Proc. Appl. Math. Mech., 17: 211-212.
2017 | The geometrical shape of mesenchymal stromal cells measured by quantitative shape descriptors is determined by the stiffness of the biomaterial and by cyclic tensile forces.
Uynuk-Ool, T., Rothdiener, M., Walters, B., Hegemann, M., Palm, J., Nguyen, P., Seeger, T., Stöckle, U., Stegemann, J. P., Aicher, W. K., Kurz, B., Hart, M. L., Klein, G., & Rolauffs, B. (2017). The geometrical shape of mesenchymal stromal cells measured by quantitative shape descriptors is determined by the stiffness of the biomaterial and by cyclic tensile forces. Journal of tissue engineering and regenerative medicine, 11(12), 3508–3522.
2017 | Engineering the geometrical shape of mesenchymal stromal cells through defined cyclic stretch regimens.
Walters, B., Uynuk-Ool, T., Rothdiener, M., Palm, J., Hart, M. L., Stegemann, J. P., & Rolauffs, B. (2017). Engineering the geometrical shape of mesenchymal stromal cells through defined cyclic stretch regimens. Scientific reports, 7(1), 6640.
2018 | Chondrocyte migration in an acellular tissue‐engineered cartilage substitute.
Nachtsheim, J., Dursun, G., Markert, B. and Stoffel, M. (2018), Chondrocyte migration in an acellular tissue‐engineered cartilage substitute. Proc. Appl. Math. Mech., 18: e201800425.
2019 | Experimental Study on Cell-free Approach for Articular Cartilage Treatment, Current Directions in Biomedical Engineering.
Dursun, G., Markert, B., & Stoffel, M. (2019). Experimental Study on Cell-free Approach for Articular Cartilage Treatment, Current Directions in Biomedical Engineering, 5(1), 171-174.
2019 | Trefoil Factor 3 (TFF3) Is Involved in Cell Migration for Skeletal Repair.
Krüger, K., Schmid, S., Paulsen, F., Ignatius, A., Klinger, P., Hotfiel, T., Swoboda, B., & Gelse, K. (2019). Trefoil Factor 3 (TFF3) Is Involved in Cell Migration for Skeletal Repair. International journal of molecular sciences, 20(17), 4277.
2019 | Chondrocyte colonisation of a tissue-engineered cartilage substitute under a mechanical stimulus.
Chondrocyte colonisation of a tissue-engineered cartilage substitute under a mechanical stimulus.
2020 | Compression Bioreactor-Based Mechanical Loading Induces Mobilization of Human Bone Marrow-Derived Mesenchymal Stromal Cells into Collagen Scaffolds In Vitro
Medical Faculty Mannheim, Heidelberg University, 68167 Mannheim, Germany;
Carolina.Gamez@medma.uni-heidelberg.de (C.G.); Baerbel.Schneider6@gmx.de (B.S.-W.);
as.work@aikq.net (A.S.)
2020 | Complex mechanical behavior of human articular cartilage and hydrogels for cartilage repair
ProMatLeben – Verbundprojekt
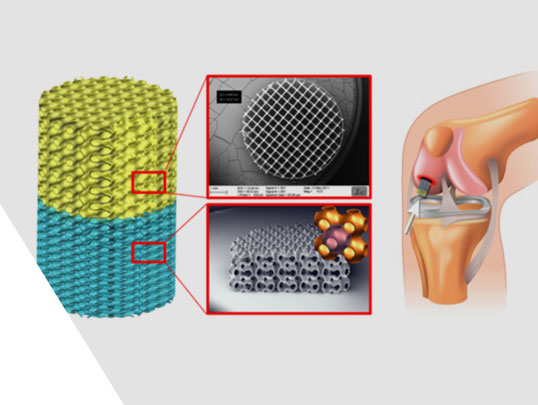
Erforschung eines industriellen laserbasierten Nano-3D-Druckverfahrens für hierarchisch strukturierte Knorpel-Knochen-Implantate auf Polymerbasis (Poly-IMPLANT-Druck)
- Mathys Orthopädie GmbH: Erforschung implantatspezifischer chirurgischer Instrumente
- IBA Heiligenstadt e.V.: Erforschung von Photopolymeren und 3D-Gerüsten
- Multiphoton Optics GmbH: Erforschung eines Zwei-Photonen-Polymerisationsprozesses zur Herstellung des Implantats.
- meidrix biomedicals GmbH: Erforschung der Kollagenfunktionalisierung der Implantate
- Universität Gießen: Erforschung der osteogenen Differenzierungsfähigkeit im Implantat.
Das Ziel des Verbundprojekts Poly-IMPLANT-Druck ist es, biphasische Trägerstrukturen auf Basis biokompatibler Polymere für die optimale Versorgung von Knochen-Knorpel-Defekten zu erarbeiten: Die Trägerstrukturen sollen über geeignete knorpel- und knochenspezifische geometrische, biomechanische und biochemische Eigenschaften verfügen. Hierbei können sich die Strukturen der Knorpel- und Knochenphasen unterscheiden. Die 2PP-Technik als variable 3D-Drucktechnik in Verbindung mit einem automatisierten Fertigungsprozess stellt den Schlüssel zur gezielten Mikrostrukturierung eines 3D-Trägerkonstruktes in Kombination mit der Einstellung der Materialsteifigkeit, der Bioaktivität der Trägeroberflächen, der Simulation der Extrazellulären Matrix (ECM) und der Degradationsgeschwindigkeit dar.
Projektfakten und weiterführende Links:
- Laufzeit: 01.05.2019 – 30.04.2022
- Projektlink: www.promatleben.de/de/projekte/projekte-alphabetisch/poly-implant-druck
- Programm ProMatLeben: www.promatleben.de des BMBFs www.bmbf.de
- Projektträger: VDI Projekt GmbH www.vditz.de
- Gefördert durch: Bundesministerium für Bildung und Forschung (BMBF) www.bmbf.de
ZIM-Kooperationsprojekt
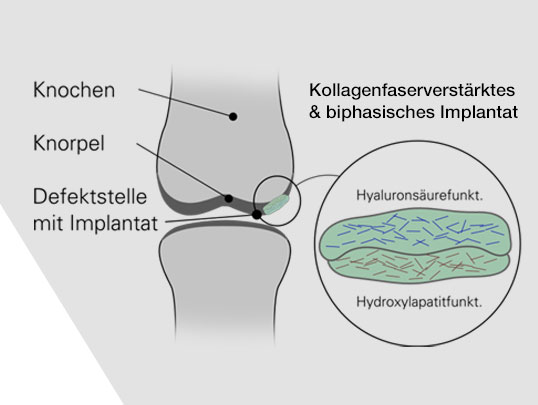
Entwicklung eines kollagenfaserverstärkten und biphasischen Implantates zur Knorpelregeneration
meidrix biomedicals GmbH und das Institut für Textilmaschinen und textile Hochleistungswerkstofftechnik (ITM) der TU Dresden sind Partner eines Kooperationsprojekts im Rahmen des Zentralen Innovationsprogramms Mittelstand (ZIM) des Bundesministeriums für Wirtschaft und Energie.
Ziel des ZIM-Kooperationsprojekts ist die Entwicklung von neuartigen funktionalen und biphasischen Kollagenfaserimplantaten zur Gelenkknorpelregeneration.
Projektziel ist die Entwicklung eines mit funktionalisierten Kollagenfasern verstärkten, zellfreien und resorbierbaren Implantats zur Knorpelregeneration im Knie. Dieses biphasische Implantat mit schichtweisem Aufbau soll aus zwei Teilen bestehen: einem dem Knochen und einem dem Knorpel zugewandten Teil. Beide Teile bestehen aus einem mit Kollagenfasern verstärkten Kollagengel, wobei die nassgesponnenen Kollagenfasern je nach Schicht unterschiedlich funktionalisiert sind. Sowohl die Funktionalisierung als auch der biphasische Aufbau des Implantates orientieren sich streng an dem Aufbau des natürlichen Knorpels und der Grenzfläche Knochen/Knorpel.
Durch die biphasische Strukturierung des Implantats soll eine signifikante Verbesserung der Knorpelregenration und durch die Faserverstärkung eine höhere Belastbarkeit im Vergleich zu bisher verfügbaren Produkten erreicht werden.
Projektfakten und weiterführende Links:
- Laufzeit: 01.03.2019 – 28.02.2021
- Projektpartner: TU Dresden, Institut für Textilmaschinen und textile Hochleistungswerkstofftechnik (ITM), Ansprechpartner: Frau Dr.-Ing. Dilbar Aibibu, Herr Robert Tonndorf
- Programm: Zentrales Innovationsprogramm Mittelstand (ZIM) www.zim.de
- Projektträger: AiF Projekt GmbH www.aif-projekt-gmbh.de
- Gefördert durch: Bundesministeriums für Wirtschaft und Energie (BMWi) www.bmwi.de
Weitere Partner

Fraunhofer Institut
www.igb.fraunhofer.de

BBF Sterilisationsservice GmbH

BioRegio STERN Management GmbH



